Concepto de aminas
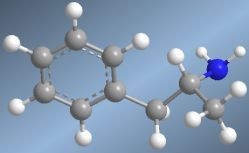 Las aminas son sustancias, derivadas del amoníaco, caracterizadas por ser polares en forma moderada, con mayor punto de ebullición que los alcanos pero inferiores al punto de los alcoholes. Sobre el átomo de hidrógeno, las aminas poseen un par de electrones no compartidos. Según se considere sustituido uno, dos o tres átomos de hidrógeno por radicales alquilo o arilo, se originan las aminas primarias, secundarias y terciarias, respectivamente. Si se sustituyen por arilo aparecen las aminas aromáticas.
Las aminas son sustancias, derivadas del amoníaco, caracterizadas por ser polares en forma moderada, con mayor punto de ebullición que los alcanos pero inferiores al punto de los alcoholes. Sobre el átomo de hidrógeno, las aminas poseen un par de electrones no compartidos. Según se considere sustituido uno, dos o tres átomos de hidrógeno por radicales alquilo o arilo, se originan las aminas primarias, secundarias y terciarias, respectivamente. Si se sustituyen por arilo aparecen las aminas aromáticas.
En las aminas primarias y secundarias, sus moléculas pueden constituir con el agua y entre sí, fuertes enlaces de hidrógeno. Las terciarias, solo con el agua pero no entre sí, es por ello que estas últimas hierven a menor temperatura que las primeras, aunque tengan un peso molecular comparable. Las aminas de poco peso molecular, son muy solubles en agua.
Por su naturaleza nucléofila, a causa del par de electrones no compartidos del átomo de nitrógeno y por su basicidad, son reactivas. Las primarias y secundarias dan lugar a sales alquiloamónicas al reaccionar con halogenuros de alquilo, formando las sulfonamidas cuando reaccionan con los cloruros de ácidos sulfónicos; y todas forman sales de amonio solubles en agua al reaccionar con ácidos inorgánicos. Las terciarias no son reactivas con el ácido nitroso.
La denominación de las aminas primarias se conforma mediante la especificación del grupo orgánico unido al nitrógeno sumando la terminación “amina” (Metilamina, Etilamina, Isobutilamina, Pert-Butilamina, Bencilamina y Alilamina). En as aminas secundarias y terciarias se designan los grupos orgánicos, en modo individual o usando los prefijos di o tri, si son iguales. (Metil etil amina, Dietilamina, Di-sec-butilamina, Etilbencilamina, Trietilamina).
En las sales de aminas y de los compuestos cuaternarios de amonio, los nombres se componen adicionando al nombre del anión, la terminación amonio, por ejemplo Bromuro de trimetilamonio.
Fingermann, H. (24 de febrero de 2013). Concepto de aminas. Deconceptos.com. https://deconceptos.com/ciencias-naturales/aminas
| Concepto siguiente >> |